Vídeo tuturial hidruros
sábado, 13 de agosto de 2016
HIDRUROS
Los hidruros son compuestos binarios formados por átomos de hidrógeno y de otro elemento (pudiendo ser este, metal o no metal). Existen dos tipos de hidruros: los metálicos y los hidrácidos.
LOS HIDRUROS METÁLICOS
Son el resultado de la unión entre el hidrógeno y un elemento metálico Metal + hidrógeno = hidruro metálico
2Na + H2 ------ 2NaH
La fórmula de un hidruro metálico es del tipo MHn donde:
· M es el símbolo de un elemento metálico.
· H es el símbolo del hidrógeno.
· n es el subíndice del hidrógeno.
Para nombrar a un hidruro metálico a partir de su fórmula lo podemos hacer siguiendo dos nomenclaturas distintas:
NOMENCLATURA SISTEMÁTICA
El nombre sistemático es del tipo:
Prefijo + hidruro de nombre del elemento
Donde:
· El nombre del elemento lo obtendremos del símbolo (M) que aparece en la fórmula.
· El prefijo de la palabra hidruro lo obtendremos del subíndice del hidrógeno (n) que aparece en la fórmula
subíndices
|
prefijos
|
sin subíndice
|
mono (*)
|
2
|
di
|
3
|
tri
|
etc.
|
etc.
|
(*) el prefijo mono puede omitirse
| |
Para escribir la formula de un hidruro metálico primero se escribe el símbolo del elemento metálico (parte positiva) y después el de hidrógeno (parte negativa).
EJEMPLO
DIHIDRURO DE CALCIO
NOMENCLATURA STOCK
El nombre de Stock es del tipo:
Hidruro + de nombre del elemento + (valencia)
Donde:
· El nombre del elemento lo obtendremos del símbolo (E) de la fórmula.
· La valencia, que va entre paréntesis y con numeración romana, coincide con el subíndice del hidrógeno (n).
. LOS HIDRUROS NO METÁLICOS E HIDRÁCIDOS
Los hidrácidos (compuestos binarios ácidos) e hidruros no metálicos son compuestos formados entre el hidrógeno y un no metal de las familias VIA y VIIA .
La fórmula de un hidrácido es del tipo HnX
· X es el símbolo de un elemento de los grupos XVI o XVII.
· H es el símbolo del hidrógeno.
· n es el subíndice del hidrógeno
Para nombrar a un hidrácido a partir de su fórmula, lo podemos hacer siguiendo dos nomenclaturas distintas
NOMENCLATURA SISTEMÁTICA
El nombre sistemático es del tipo:
Nombre del elemento + uro de hidrógeno
Donde el nombre del elemento lo obtendremos del símbolo (X) que aparece en la fórmula.
EJEMPLO:
SULFURO DE HIDRÓGENO
NOMENCLATURA TRADICIONAL
El nombre clásico es del tipo:
Ácido de + nombre del elemento + hídrico
EJEMPLO:
No metal + Hidrógeno → Hidruro no metálico
Cl2 + H2 → 2HCl
Los hidrácidos provienen de disolver en agua a los hidruros no metálicos y por esa misma razón son estos los que se encuentran en estado acuoso. Se nombran con la palabra ácido, como nombre genérico, y como nombre específico se escribe el nombre del no metal y se le agrega el sufijo –hídrico. Al igual que en estado gaseoso el nombre genérico es nombrado por el elemento más electropositivo.
Hidruro No metálico + Agua → Hidrácido
HCl(g) + H2O → H+1 + Cl-1
HIDRÓXIDOS
Los hidróxidos son un grupo de compuestos químicosformados por un metal y uno o varios anioneshidroxilos, en lugar de oxígeno como sucede con losóxidos.
La formula de un hidróxido es del tipo M(OH)n donde:
· M es el símbolo del metal.
· OH es el ion hidróxido.
· n es el subíndice del ion hidróxido que nos indica el número de iones hidróxido que acompañan a un ion del metal.
Para nombrar a un hidróxido a partir de su fórmula, lo podemos hacer siguiendo dos nomenclaturas distintas
NOMENCLATURA SISTEMÁTICA
El nombre sistemático es del tipo:
Prefijo + hidróxido de nombre del metal
Donde
· El nombre del metal lo obtendremos del símbolo (M) que aparece en la fórmula.
· El prefijo inicial lo obtendremos del subíndice del ion hidróxido (n) que aparece en la fórmula.
subíndices
|
prefijos
|
sin subíndice
|
mono (*)
|
2
|
di
|
3
|
tri
|
etc.
|
etc.
|
(*) el prefijo mono puede omitirse
| |
EJEMPLO
NOMENCLATURA STOCK
El nombre de Stock es del tipo:
Hidróxido + de + nombre del metal + (valencia en número romano)
Donde:
· El nombre del metal lo obtendremos del símbolo (M) de la fórmula.
· La valencia es la del metal, que va entre paréntesis y con numeración romana, lo obtendremos del subíndice (n) que aparece en la fórmula
EJEMPLO
NOMENCLATURA TRADICIONAL
Cuando un elemento presenta dos estados de oxidación diferentes, el nombre termina en oso en los compuestos en que el elemento tiene la menor valencia y en ico en los que el elemento tienen la mayor valencia
EJEMPLO:
Ni(OH)2 = Hidróxido niqueloso
|
Ni (OH)3 = Hidróxido niquelico
|
lunes, 4 de abril de 2016
domingo, 20 de marzo de 2016
Estado de oxidación (CO)
Es el indicador del grado de oxidación de un átomo que forma parte de un compuesto u otra especie química. Formalmente, es la carga eléctrica hipotética que el átomo tendría si todos sus enlaces con elementos distintos fueran 100% iónicos. El EO es representado por números, los cuales pueden ser positivos, negativos o cero. En algunos casos, el estado de oxidación promedio de un elemento es una fracción, tal como +8/3 para el hierro en la magnetita (Fe3O4). El mayor EO conocido es +8 para los tetroxidos de rutenio, xenón, osmio, iridio, hassio y algunos complejos de plutonios, mientras que el menor EO conocido es -4 para algunos elementos del grupo del carbono
La oxidación se da cuando un elemento o compuesto pierde uno o más electrones. Generalmente, cuando una sustancia se oxida (pierde electrones), otra sustancia recibe o capta dichos electrones reduciéndose. Este es el mecanismo básico que promueve las reacciones de óxido-reducción o redox.
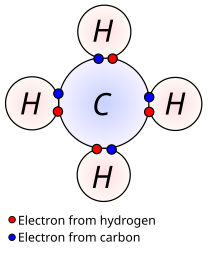
Un átomo tiende a obedecer la regla del octeto para así tener una configuración electrónica igual a la de los gases nobles, los cuales son muy estables eléctricamente. Dicha regla sostiene que un átomo tiende a tener ocho electrones en su nivel de energía más externo. En el caso del hidrógeno este tiende a tener 2 electrones, lo cual proporciona la misma configuración electrónica que la del helio.
Cuando un átomo A necesita,
por ejemplo, 3 electrones para obedecer la regla del octeto, entonces dicho
átomo tiene un número de oxidación de -3. Por otro lado, cuando un átomo B tiene
los 3 electrones que deben ser cedidos para que el átomo A cumpla la ley del
octeto, entonces este átomo tiene un número de oxidación de 3+. En este ejemplo
podemos deducir que los átomos A y B pueden unirse para formar un compuesto, y
que esto depende de las interacciones entre ellos. La regla del octeto y del
dueto pueden ser satisfechas compartiendo electrones (formando moléculas)
o cediendo y adquiriendo electrones (formando compuestos de iones).
Suscribirse a:
Entradas (Atom)